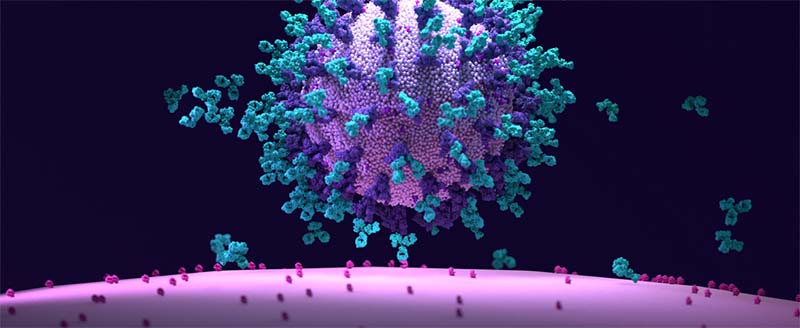
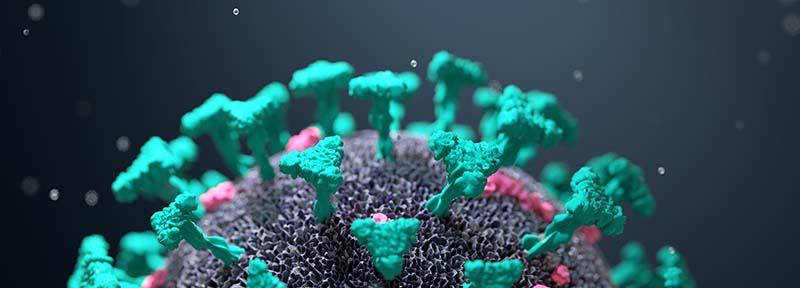
RNA 발현의 공간적 시각적 분석 - ISH 분석서비스

DNA, RNA 및 단백질등의 바이오마커는 기본 세포 기능을 이해하고 임상 질환을 진단하며 최적의 치료법을 식별하기 위한 강력한 도구입니다. 특히, RNA는 유기체에서 발생하는 동적 유전자 발현 변화를 확인하는 이상적인 지표입니다. ACD사에서는 손상되지 않은 조직 내 단일 세포 수준의 in situ 유전자 발현을 포착하는 ISH 분석서비스를 제공합니다. 이 방법은 세포 간 상호 작용을 더 잘 이해하기 위해 형태학적 맥락에서 분자를 검출합니다. RNAscope ISH 분석은 특허받은 신호 증폭 및 백그라운드 신호 억제 기술을 기반으로 하며 기존 RNA ISH에 비해 특이성과 민감도가 크게 향상됩니다. 가장 대표적인 RNAscope ISH 분석 사례를 소개합니다. 1. Single Cell Analysis 단일 세포 RNA 시퀀싱(scRNA-Seq)으로 개별 세포의 전사체 프로필을 특성화하는 것은 알려진 세포 유형과 새로운 세포 유형을 식별하고 조직 구조와 기능을 이해하는 보편적인 도구가 되어 단일 세포 생물학의 새로운 시대를 열었습니다. 이는 특히 포유류 뇌 및 종양과 같이 세포 이질성이 높은 복잡한 기관 및 조직에서 사실임이 입증되었습니다. 그러나 scRNA-Seq는 분리된 세포를 활용하므로 분석 중인 세포 집단의 공간 조직이 손실됩니다. 따라서 단일 세포 및 공간적 유전자 발현 모두를 시각적으로 확인하기 위해 RNA in situ hybridization(ISH)과 같은 방법으로 scRNA-seq 분석을 보완하는 것이 필수적입니다. RNAscope Assay는 강력하고 특이성이 높으며 민감한 멀티플렉스 RNA ISH assay로, 높은 처리량의 단일 세포 전사체 결과를 시각화할 수 있습니다. 단일 세포 수준에서 최대 4개의 특정 마커를 이용하여 최대 4개의 다중분석을 수행할 수 있습니다 (IHC와 결합 가능). 이러한 분석을 통해 단일 세포 내의 개별 유전자 및 유전자 시그니처 발현 프로필을 시각적으로 확인할 수 있으므로 전사 결과를 검...